NOTICIAS
Resumen: IX Congreso Nacional de la Sociedad Española de EC

La Sociedad Española de Enfermedad Celíaca, fundada en 2008, celebra un congreso nacional cada dos años en el que se reúnen médicos e investigadores de diferentes disciplinas para poner en común los últimos avances y futuros retos en torno a esta patología y su tratamiento. Bilbao fue la sede de la 9ª edición, que tuvo lugar el pasado mes de noviembre.
El trigo
Un cultivo milenario
El 70% de los agricultores del planeta cultivan cereales. Históricamente, el cultivo de trigo y cebada procede del Próximo Oriente, el arroz del Lejano Oriente, el maíz de la América Precolombina y el sorgo de África. Destaca entre todos ellos el trigo, que se sitúa en la base de las sociedades organizadas, siendo su principal fuente de alimentación. La construcción de la pirámide de Keops, en Egipto, ocupó al menos a 20.000 trabajadores durante 20 años. Su alimentación supuso la molienda de toneladas y toneladas de grano y la producción de cientos de kilos de pan cada día en la que pudieron intervenir hasta 300 panaderos. Hoy, el trigo sigue siendo la base de la alimentación humana. La especie más cultivada es el trigo panadero (94%), seguida del trigo duro (5%) y de otras especies minoritarias (1%), que en total suman unas 30.000 líneas diferentes.
El origen evolutivo de los cereales se remonta 100 millones de años atrás. Hace 20 millones de años se diversificó el arroz y hace 4 millones de años se separó el ancestro común a trigo, cebada, centeno y avena. Con el comienzo de la agricultura en el Neolítico, hace unos 10.000 años, especies antiguas y silvestres del trigo comenzaron a ser cultivadas en Oriente Medio, como el Einkorn o escanda menor (Triticum monococcum), que era una especie diploide con 7 pares de cromosomas (genoma AA). El cruce de dos linajes diploides ancestrales (AA y BB) dio origen al Emmer o farro (Triticum dicoccoides), antepasado del actual trigo duro (genoma AABB), cuya harina se usa en la elaboración de la pasta. Y la hibridación espontánea de los nuevos tetraploides con un tercer diploide ancestral (DD) dio lugar a los hexaploides espelta y trigo harinero (Triticum aestivum, genoma AABBDD), cuyas harinas son empleadas en la elaboración del pan. En todo este proceso, 3 mutaciones espontáneas fueron cruciales para convertir el trigo en un cultivo productivo: una transformó un raquis quebradizo en otro más estable que impedía la caída del grano durante la cosecha, otra dio lugar a un grano descascarado que favorecía su molienda y una tercera redujo la altura de la espiga.
Así lo expuso Francisco Barro (Instituto de Agricultura Sostenible -IAS- del CSIC, Córdoba) en la conferencia inaugural del Congreso, quien destacó también que el trigo es un reservorio nutritivo que aporta proteínas, carbohidratos, fibra soluble e insoluble, vitaminas, minerales y antioxidantes. Es el único cereal panificable gracias a que su grano, y por tanto sus harinas, contiene gluteninas de alto peso molecular, uno de los componentes del gluten que tiene estructura de muelle y la posibilidad de establecer puentes disulfuro entre aminoácidos de cisteína que permiten construir una malla elástica muy útil en la panificación. La viscosidad de las masas es aportada por el otro componente del gluten, las gliadinas, donde reside la toxicidad de esta proteína. En concreto, la fracción alfa de las gliadinas contiene la secuencia de aminoácidos que resulta más tóxica para las personas con enfermedad celíaca (EC) y que lo es para todas ellas, el conocido como péptido 33mer.
En busca de un trigo sin gluten
El estudio evolutivo de los genes de las gliadinas arroja datos interesantes, continúa el Dr. Barro. Las gliadinas más tóxicas, correspondientes a las fracciones alfa y gamma, no están presentes en el genoma DD y por tanto no se encuentran en el trigo duro (el tetraploide AABB). Y en contra de lo que se solía pensar, los trigos más modernos no son más tóxicos que sus antepasados, sino al contrario, pues el recorrido evolutivo desde los trigos diploides ancestrales hasta los trigos hexaploides actuales ha incrementado su proporción de gluteninas frente a las gliadinas, por la selección gradual de las variedades con mejores propiedades panificables. El análisis de variedades de trigo cultivadas desde el siglo XIX hasta nuestros días así lo atestigua. Algo similar se ha comprobado en las cebadas y los centenos que se cultivan actualmente al comparar con sus variedades silvestres.
Reducir o eliminar la toxicidad de los trigos actuales por métodos clásicos de hibridación y selección es inviable dada la enorme complejidad genética de estas especies, tetraploides o hexaploides, con multitud de genes implicados en la síntesis del gluten que contienen secuencias tóxicas repartidas por todos los genomas (AA, BB, DD). La técnica de ingeniería genética del ARN de interferencia (ARNi) ha permitido silenciar los genes de las gliadinas hasta reducir en un 98% la toxicidad de las harinas, evidenciada por su menor reactividad frente al anticuerpo G12, específico contra el péptido 33mer. Las líneas obtenidas mantienen constante el contenido proteico total de su grano, lo que implica un cambio en la composición de aminoácidos para compensar la falta de gliadinas. Aumenta, por ejemplo, la lisina, uno de los aminoácidos esenciales en nuestra dieta.
Se trata, no obstante, de especies transgénicas que tienen muy difícil su aprobación para ser cultivadas en la Unión Europea. La tecnología de edición genética CRISPR/Cas9 puede sortear la consideración de transgénico si las líneas obtenidas son viables y no superan un determinado número de mutaciones, lo que supone modificar por separado grupos de genes (alfa, gamma y omega gliadinas) para después cruzar entre sí las líneas mutadas con la esperanza de lograr híbridos que reúnan en una misma variedad las mutaciones generadas en cada grupo de genes.

Componentes beneficiosos del trigo: la fibra
Jara Pérez (Instituto de Ciencia y Tecnología de Alimentos y Nutrición -ICTAN- del CSIC, Madrid) centró su intervención en la fibra de trigo. En 2017 se produjeron en el mundo 1 millón de muertes asociadas a dietas bajas en fibra, cuya ingesta recomendada es de 25-30 gramos al día, aunque basta con 10 gramos diarios de fibra para tener un buen tránsito intestinal. A partir de ahí, a mayor ingesta, mayor beneficio para la salud. Se reduce, por ejemplo, el riesgo de desarrollar diabetes tipo 2. Pero hay que tener en cuenta también que la adición de más fibra en un alimento puede llevar aparejada la adición de más grasa para mejorar su palatabilidad, como ocurre con las galletas comercializadas como digestive.
El efecto beneficioso de la fibra no se debe solo a los carbohidratos fermentables, sino también a los polifenoles que la acompañan y a los ácidos grasos de cadena corta que se generan por la fermentación de la fibra soluble por parte de las bacterias intestinales, además de otras sustancias, denominadas postbióticos, como los arabinoxilanos, también sustrato de fermentación bacteriana.
En cuanto a las denominaciones y sus beneficios para la salud, está demostrado que el consumo de alimentos elaborados con cereales integrales es beneficioso y es necesario recordar que el pan integral es aquel elaborado con harina 100% integral, lo que no significa que el pan sea 100% integral pues la harina suele representar el 60-70% del total de sus componentes. El salvado de trigo no computa a la hora de establecer el porcentaje de harina integral. En los países nórdicos se aconseja el consumo de 90 gramos de cereales integrales al día. La mayoría de los países no alcanzan esa cantidad, España se encuentra en la parte baja de la tabla.
Sobre el pan de masa madre no hay tanta evidencia y a día de hoy no se puede afirmar que su consumo tenga un efecto positivo para la salud, al menos desde el punto de vista clínico.
Componentes perjudiciales del trigo: la acrilamida
Los procesos de horneado, tostado y extrusión de alimentos basados en cereales, ya sea en la industria, en la restauración colectiva o en el ámbito doméstico, genera sustancias positivas, relacionadas con en el sabor o el aroma en el producto final, pero también sustancias perjudiciales. Marta Mesías (Instituto de Ciencia y Tecnología de Alimentos y Nutrición -ICTAN- del CSIC, Madrid) destacó la acrilamida (un derivado suyo, la glicinamida, es cancerígena), que resulta de la conocida como reacción de Maillard, por la interacción entre componentes azucarados y componentes proteicos del alimento cuando éste es sometido a temperaturas superiores a los 120ºC en condiciones de baja humedad. Este compuesto no debe superar ciertos límites establecidos por la Agencia Europea de Seguridad Alimentaria (EFSA) y es especialmente relevante en los cereales, las patatas y el café. Como ejemplo, es más segura una patata cocida (sometida a temperaturas de unos 100ºC con alta humedad) que una patata frita (sometida a temperaturas muy superiores a los 120ºC con escasa humedad). En cuanto a seguridad, de menor a mayor toxicidad por este motivo irían el arroz, el trigo, la cebada, el maíz, el trigo integral, la avena y el centeno.
Factores implicados en la enfermedad celíaca
Permeabilidad intestinal
El ratio lactulosa/manitol en orina es un buen indicador del estado de permeabilidad del epitelio intestinal. La lactulosa es un azúcar sintético de difícil absorción por su tamaño, se absorbe como mucho a nivel de las criptas, mientras que el manitol, más pequeño, se absorbe bien. El aumento de permeabilidad intestinal implica una mayor absorción de lactulosa, pero no de manitol, lo que aumenta el ratio lactulosa/manitol. La expresión de genes relacionados con las uniones estrechas, como IRF7, se puede estudiar en saliva y se correlaciona bien con el ratio lactulosa/manitol, por lo que puede ser una prueba fiable del estado de permeabilidad del intestino. Así se ha comprobado al estudiar sujetos con EC activa, EC tratada con dieta sin gluten a los 6 meses y a los 2 años, y sin EC. Hay que tener en cuenta que la absorción de manitol se ve reducida por la atrofia de vellosidades. Lo explicó Silvia Martín (Instituto de Investigación Sanitaria Biobizkaia, Bilbao).
Factores genéticos
Iris Jonkers (Universidad de Groningen, Países Bajos) investiga alteraciones de la expresión génica en la mucosa intestinal. Comentó que hay descritos 118 genes fuera de la región HLA relacionados con la inflamación que se expresan de forma diferente en las células epiteliales intestinales en enfermedades como la EC, la enfermedad de Crohn o la colitis ulcerosa. Su expresión no solo afecta a células inmunitarias. Unos tienen una expresión más activa y están relacionados con la presentación antigénica por parte de los enterocitos, mientras que otros tienen una expresión menos activa, en parte debido también a la pérdida de tejido que supone la atrofia vellositaria y están relacionados con la absorción de nutrientes, que se ve mermada.
En esta misma línea, Ainara Castellanos (Universidad el País Vasco, Bilbao) se centró en la epitranscriptómica, que estudia las modificaciones rápidas y reversibles en el ARN, en las que participan 3 familias de proteínas conocidas en este campo como writers, readers e erasers (traducido equivaldría a escritoras, lectoras y borradoras). Estos ARN ejercen una función reguladora de la expresión génica gracias a la estructura tridimensional que adquieren cuando se pliegan, que permite bloquear o desbloquear la expresión de los genes que regulan. Mutaciones en estos ARN pueden afectar a la manera en que se pliegan y por tanto alterar su función de control de la expresión génica.
Las metilaciones son una de las principales modificaciones que afectan a la regulación de la expresión génica. Se ha demostrado que el gluten es capaz de incrementar procesos de metilación y con ello favorecer procesos inflamatorios. En EC se han identificado diferentes mutaciones que afectan a la maquinaria implicada en estas metilaciones provocando una desregulación de la expresión de genes vinculados con la inflamación, favoreciéndola. Compuestos naturales de alimentos como la cúrcuma o la salvia contienen sustancias, como el ácido salvianólico en ésta última, capaces de corregir esta desregulación de la inflamación al actuar sobre la maquinaria implicada en las metilaciones revirtiendo el efecto proinflamatorio de las citadas mutaciones.
Factores ambientales
África Sanchiz (Universidad de León) investiga el papel de las infecciones digestivas como detonantes de la EC. Comparando las biopsias de pacientes con EC activa y EC potencial se observa que en un porcentaje de los casos con EC activa puede detectarse la expresión de genes vinculados con la defensa frente a virus intracelulares. El papel de estos patógenos se está estudiando en ratones en los que se intenta inducir la EC administrando solo gluten, solo virus o ambos factores a la vez.
Y también se investiga el posible papel del gluten durante la etapa prenatal. Es posible detectar gluten en el líquido amniótico de mujeres embarazadas, sin diferencias entre el segundo o el tercer trimestre. No así en mujeres celíacas embarazadas que hacen dieta sin gluten. Se ha detectado correlación entre la cantidad de gluten en líquido amniótico y en orina, y también una relación dinámica con la alimentación: no se detecta en el líquido amniótico tras una cesárea programada pero sí si la cesárea es de urgencia, sin ayuno previo. Lo expuso Lourdes Moreno (Universidad de Sevilla) y continuó Ángela Ruiz (Universidad de Sevilla) con la detección de gluten en la leche materna. Puede detectarse en mujeres sin EC, y correlaciona con los niveles detectados en orina. Tras una prueba de provocación con gluten en mujeres sin EC previamente puestas a dieta sin gluten se detecta gluten en orina hasta 24 horas después de la ingesta y en la leche materna hasta 72 horas después de la ingesta.

Epidemiología de la enfermedad celíaca
Para conocer la prevalencia clínicamente probada de la EC no valen los registros sanitarios y son necesarios estudios poblacionales que eviten sesgos de selección (donantes de sangre, colegios, etc.) y que incluyan entre 20.000 y 30.000 sujetos, tal como relató María Esteve (Hospital Mutua de Terrassa, Barcelona). Los estudios de seroprevalencia realizados en España hasta la fecha, 7 en total, adolecen de ello y han arrojado cifras que oscilan entre el 0,26% y el 3,03%. Según indican los metaanálisis más recientes, la incidencia de la EC se ha incrementado un 7,5% en el mundo. Sin embargo, los resultados de 3 estudios de prevalencia llevados a cabo en Cataluña en las últimas dos décadas contradicen esa tendencia. Se realizaron con la misma metodología y consistía en realizar el cribado entre personas que acudían al hospital para alguna cirugía menor, de tipo ambulatoria. El primero incluyó a 4.230 personas de 1 a 80 años (780 en edad pediátrica) entre 2004 y 2007. El segundo, de 2013 a 2017, estudió a 3.659 niños de 1 a 5 años. El tercero reclutó a 5.330 personas de 1 a 80 años entre 2020 y 2023, con 364 niños. De ellos se observó un descenso en la prevalencia de la EC infantil que pasó de 1/35 en el primer periodo a 1/66 en el tercero. Evaluando de forma retrospectiva posibles factores ambientales que hayan condicionado ese descenso se identificó como principal candidato la vacunación frente al rotavirus, que se empezó a administrar en Cataluña en el año 2006, alcanzando una tasa de vacunación del 50% en el segundo periodo estudiado.
Enfermedad celíaca en la edad pediátrica
Enfermedad celíaca potencial
Aproximadamente el 10% de los pacientes pediátricos con EC encajan en el diagnóstico de EC potencial, definida por la elevación de anticuerpos específicos en sangre en ausencia de atrofia de vellosidades intestinales, siendo positiva la predisposición genética HLA, con o sin síntomas. Según el registro de Renata Auricchio (Universidad Federico II de Nápoles, Italia), los pacientes con EC potencial tienen una edad mediana de 6 años, el 67% son de sexo femenino, normalmente son portadores de una sola copia de la variante de riesgo HLA-DQ2, tienen niveles bajos de anticuerpos IgA antitransglutaminasa (TG2) en sangre y muestran elevación de linfocitos T gamma-delta en las biopsias duodenales, incluso en los casos sin lesión histológica (Marsh 0). Aquellos que no presentan síntomas pueden mantener la dieta con gluten por tiempo indefinido (con controles periódicos) sin riesgo para su salud, al no afectar a su estado nutricional ni incrementar el riesgo de sufrir problemas autoinmunes mientras la EC siga en estado potencial.
En los casos con síntomas, en cambio, es aconsejable que inicien la dieta sin gluten, aunque los síntomas solo remiten en la mitad de ellos, lo que indica que es frecuente que los síntomas inicialmente atribuidos a la EC no tengan nada que ver con la patología.
La EC potencial se caracteriza por una inflamación intestinal de bajo grado con un mayor ratio IL10/IFNgamma y niveles más bajos de IL15 e IL21 en comparación con la EC activa. Recuerda mucho a la EC de bajo grado descrita por Ferguson en 1993, definida generalmente en familiares de pacientes con EC en los que se observaba elevación de anticuerpos anti-TG2 en sangre y aumento de linfocitos intraepiteliales, con elevación del subtipo T gamma-delta, en ausencia de atrofia de vellosidades.

Enfermedad celíaca ultracorta
La EC ultracorta se caracteriza por mostrar lesión intestinal únicamente en el bulbo duodenal (primer tramo del duodeno). Aproximadamente el 10% de los casos diagnosticados actualmente de EC presentan atrofia de vellosidades únicamente en dicho tramo proximal del duodeno, mientras que las biopsias de duodeno distal son completamente normales o muestran como mucho una linfocitosis intraepitelial sin atrofia (lesión Marsh tipo 1). Según los datos disponibles, expuestos por Gemma Castillejo (Hospital Sant Joan de Reus, Tarragona), la edad de debut de esta forma de EC es de 5 a 7 años y son casos que muestran poca sintomatología. Presentan niveles más bajos de anticuerpos IgA anti-TG2 en sangre y el linfograma intraepitelial puede mostrar un patrón de EC completo o parcial en proporción similar a la que se observa en la EC convencional.
En 2001 se empezó a plantear la necesidad de tomar biopsias del duodeno proximal, no solo del distal. En 2004 se describió la lesión intestinal como una lesión parcheada que requiere, por tanto, la toma de varias muestras para garantizar que en al menos una de ellas se observe lesión y en 2008 se publicó que siempre hay lesiones en el bulbo. No obstante, hay que evitar confundir la enteropatía propia de la EC en el bulbo con lesiones causadas por otros motivos en esta zona tan próxima al estómago, como Helicobacter pylori o la duodenitis péptica. Y también hay que tener en cuenta que la presencia de las glándulas de Brünner y la menor longitud de las vellosidades en este tramo inicial del intestino pueden dar la impresión de atrofia vellositaria cuando en realidad la mucosa es normal.
Quedan abiertas varias cuestiones sobre esta forma de EC. ¿Se ve cada vez más porque se busca antes la EC gracias al cribado? ¿Evoluciona lentamente hacia una EC convencional o se mantiene en su forma ultracorta por tiempo indefinido? ¿Se trata de un estadío intermedio entre la EC potencial y la EC activa convencional? El linfograma intraepitelial no distingue entre unas y otras, por lo que tal vez haya que recurrir a pruebas de provocación para conocerla mejor.
Diagnóstico de enfermedad celíaca en casos con diabetes tipo 1
En niños y adolescentes con diabetes tipo 1 no se aconseja aplicar los criterios de diagnóstico de la EC sin biopsia porque son menos fiables. Como remarcó Ester Donat (Hospital La Fe, Valencia), si bien un resultado negativo de anticuerpos IgA entiendomisio permite descartar la EC en los casos con IgA anti-TG2 positivo, un doble positivo en estos anticuerpos, incluso cuando IgA anti-TG2 son muy altos, no siempre indica EC.
Déficit de IgA
El déficit aislado de IgA afecta a 1 de cada 600 personas de la población general, siendo de 10 a 20 veces más frecuente en personas con EC. El seguimiento serológico de pacientes con EC utilizando la tecnología Luminex, que evalúa la IgA total junto con los anticuerpos específicos en todos los casos ha revelado déficits transitorios de IgA en pacientes que mostraban IgA total normal en el momento del diagnóstico. Según María José Martínez Becerra (Hospital Fundación Jiménez Díaz, Madrid), ya se han documentado varios casos pediátricos, todos ellos menores de 4 años, y uno en adultos, en un varón de 47 años. Se desconoce la causa, el significado o la repercusión de este fenómeno.
Enfermedad celíaca en la edad adulta
El diagnóstico de la EC se basa, como norma, en el análisis serológico de anticuerpos específicos y en el estudio histológico de biopsias duodenales obtenidas mediante endoscopia. En algunos casos pediátricos puede llegar a omitirse la biopsia y en otros casos, fundamentalmente adultos, puede ser necesario recurrir a pruebas más avanzadas o a estrategias diagnósticas diferentes.
Actualización del protocolo de diagnóstico de la enfermedad celíaca
Los protocolos de diagnóstico requieren algoritmos sencillos y rentables, además de adecuarse lo mejor posible a las preferencias de los pacientes. En el protocolo en vigor, que está siendo actualizado en este momento, son varios los puntos a consensuar o a definir si no están recogidos en la edición actual y que repasó Miguel Montoro (Hospital San Jorge, Huesca), centrándose en los adultos.
- En los casos seropositivos con valores de anticuerpos IgA anti-TG2 10 veces superiores al valor normal discutir si es fiable realizar el diagnóstico sin biopsia en adultos como se hace en pediatría.
- En los casos seronegativos, realizar biopsia solo si la sospecha clínica es alta y se ha verificado antes que existe predisposición genética HLA, ya que es poco probable que sea EC si no hay déficit de IgA ni consumo de inmunosupresores. Valorar si procede actuar como sugieren las guías norteamericanas, en las que se aconseja la biopsia por motivos clínicos incluso sin predisposición genética HLA.
- En los casos con Marsh 1, asegurar que se han descartado otras posibles causas de enteritis linfocítica y que existen síntomas compatibles, genética HLA de riesgo, linfograma compatible o depósitos subepiteliales de IgA, así como una respuesta favorable a la dieta sin gluten, antes de confirmar la EC.
- En pacientes que ya están a dieta sin gluten sin tener confirmado el diagnóstico de la EC, realizar el estudio genético HLA y si resulta positivo continuar con una prueba de provocación estándar (8 semanas), seguida de analítica de sangre y biopsia, o bien corta (3 días) seguida de estudio de linfocitos T CD8 en sangre si la provocación no es bien tolerada.
- Otros temas a abordar son la EC no respondedora, el control de la adherencia a la dieta sin gluten, las posibles comorbilidades y la EC refractaria.

Estudio serológico de anticuerpos
En el apartado serológico, Carmen Ribes (Instituto de Investigación Sanitaria La Fe, Valencia) habló de los tests rápidos basados en tiras inmunocromatográficas a partir de una gota se sangre. La evaluación retrospectiva de 64 sueros correspondientes a personas diagnosticadas de EC y 53 sueros de personas sin EC mostró una buena correlación entre la determinación de IgA anti-TG2 por métodos serológicos convencionales y su análisis mediante estos tests, que además son semicuantitativos si se leen con un lector de intensidad de banda. Los tests rápidos empleados podían consistir en una única banda en la que se analizaba IgA+IgG anti-TG2 o bien en dos bandas, una para IgA anti-TG2 y otra para IgG antipéptidos desamidados de gliadina (DGP). Los valores predictivos positivo (PPV) y negativo (NPV) obtenidos fueron 74% y 100% en el primer caso (IgA+IgG anti-TG2), y en el segundo caso 78% y 100% para la banda IgA anti-TG2, 92% y 74% para la banda IgG anti-DGP y 96% y 100% cuando se consideron ambas bandas a la vez.
Algunos hospitales utilizan la tecnología Luminex, basada en esferas magnéticas, para detectar estos anticuerpos, habitualmente IgA total, IgA anti-TG2 e IgA anti-DGP. Es altamente sensible y la cuantificación requiere la dilución de las muestras, especialmente útil para poder monitorizar el descenso de los anticuerpos durante el seguimiento. Lo comentó Virginia Peña (Hospital Fundación Jiménez Díaz, Madrid).
Diagnóstico sin biopsia en adultos
En pediatría se ha establecido el límite de 10 veces sobre el valor normal en el resultado de anticuerpos IgA anti-TG2 para realizar el diagnóstico de la EC sin biopsia con total certeza, siempre que se verifique la positividad de anticuerpos IgA antiendomisio en una muestra diferente. Trasladar este punto de corte a los adultos es más controvertido y fue el tema abordado por Marta Molero (Hospital La Paz, Madrid). Un estudio comparativo entre los 6 test analíticos comerciales más utilizados persigue evaluar si el límite de 10 veces sobre el valor normal es válido para todos ellos, o cuál debería ser el umbral que garantice la EC con atrofia de vellosidades con una fiabilidad del 100%, así como la evolución de este marcador tras la instauración de la dieta sin gluten. Para las comparativas se optó por normalizar el resultado cuantitativo en múltiplos sobre el valor normal de cada test a nivel cuantitativo, y a nivel cualitativo en positivo o negativo según el valor obtenido superara o no el límite de 10 veces el valor normal. Se obtuvieron valores de corte que oscilaron entre 40 veces y 500 veces el valor normal, según el test, para garantizar la atrofia de vellosidades en el 100% de los casos. La mayor dificultad es que algunos tests requieren diluir la muestra para poder cuantificar los anticuerpos si estos están muy elevados y esta práctica incumple la normativa en métodos cuantitativos.
Linfograma intraepitelial
El estudio de linfocitos intraepiteliales por citometría de flujo, cuyo resultado se conoce como “linfograma intraepitelial”, permite identificar de forma fiable la EC en casos de duda diagnóstica, al existir un patrón característico casi exclusivo de la EC. La pionera y máxima experta en este campo es Garbiñe Roy (Hospital Ramón y Cajal, Madrid). Los linfocitos intraepiteliales tienen como marcadores superficiales CD45 (común a los linfocitos) y CD103 (integrina de adhesión al epitelio). Si se trata de linfocitos T, poseen además el marcador CD3 y un receptor de la célula T (TCR) del subtipo alfa-beta, acoplado al marcador CD4 si se trata de linfocitos T cooperadores o CD8 si se trata de linfocitos T citotóxicos efectores. Existe una pequeña proporción de linfocitos T con TCR del subtipo gamma-delta sin expresión de CD4 ni CD8, además de linfocitos intraepiteliales sin expresión de CD3.
El recuento de linfocitos intraepiteliales respecto al total del epitelio en el linfograma no es informativo, pero sí lo es el porcentaje de linfocitos T con receptor TCR gamma-delta y el porcentaje de linfocitos intraepiteliales sin marcador CD3 (CD3neg), ya que los primeros se elevan durante la fase activa de la EC y se mantienen elevados por tiempo indefinido a pesar de la dieta sin gluten, mientras que los segundos prácticamente desaparecen durante la EC activa, retornando a valores normales una vez instaurada la dieta sin gluten. La doble alteración constituye un rasgo característico de la EC y por tanto es recomendable realizar esta prueba garantizando el consumo de gluten en las semanas previas.
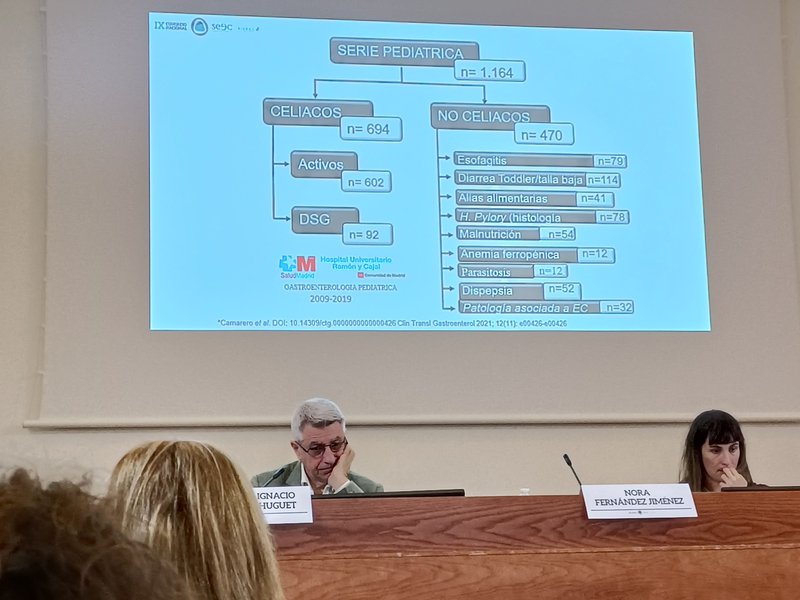
Los puntos de corte no están estandarizados y cada laboratorio los fija en base a su experiencia. La Dra. Roy, tras más de 20 años realizando y estudiando linfogramas en pacientes con EC activa y tratada con dieta sin gluten, además de en controles sin EC con patologías digestivas diversas ha establecido como límites para linfocitos T gamma-delta 15% en niños y 14% en adultos, y para linfocitos CD3neg 6% en niños y 4% en adultos. La serie pediátrica incluye 694 casos de EC y 470 controles, mientras que la serie de adultos incluye 486 casos de EC y 412 controles. Los patrones de elevación de linfocitos T gamma-delta y disminución de linfocitos CD3neg se estudian en diferentes perfiles de pacientes: EC activa, EC tratada, EC potencial, EC Marsh 1 seronegativa, además de en controles. Se han llegado a identificar patrones típicos de EC en hasta 9 controles con parásitos como Giardia y Cryptosporidium.
Prueba de provocación corta
Existen métodos que detectan marcadores tempranos de EC tras una prueba de provocación corta en sujetos que iniciaron la dieta sin gluten por su cuenta o que la siguen a pesar de un diagnóstico dudoso de EC que requiere ser verificado. En ellos se valora la movilización de células T CD4+ específicas de gluten en sangre, ya sea mediante la tecnología de los tetrámeros HLA-DQ2.5 (capturan dichas células y se detectan por citometría de flujo) o mediante ELISPOT (detecta interferón gamma producido por estas células). Concepción Núñez (Instituto de Investigación Sanitaria, Hospital Clínico San Carlos, Madrid) extrapola esta estrategia a la detección de células T CD8 en sangre dirigidas al intestino como una prueba mucho más sencilla y no limitada por los sesgos y la complejidad metodológica de las anteriores. Requiere el consumo de gluten durante 3 días y dos analíticas de sangre, una previa a la provocación y otra al sexto día. Las células T CD8 activadas son detectadas por citometría de flujo.
En un estudio con 41 pacientes con sospecha de EC en el que se aplicó el protocolo convencional de provocación de 6-8 semanas seguidas de analítica de anticuerpos específicos en sangre y biopsia intestinal con estudio de linfocitos intraepiteliales por citometría de flujo, se aprovechó para tomar una analítica de sangre basal (previa a la provocación) y otra al sexto día para valorar el incremento de linfocitos T CD8 circulantes. 8 pacientes resultaron positivos en esta prueba, 7 de ellos con linfograma característico de EC, pese a que ninguno mostró atrofia de vellosidades tras la provocación y 1 no mostraba elevación de anticuerpos específicos en sangre (no se disponía de analítica de dos de ellos, los otros 5 sí tenían anticuerpos). Hubo 4 casos con linfograma característico de EC que dieron negativo en la prueba de CD8. Si bien no es una prueba definitiva ni plenamente concluyente, se postula como mejor y más sencilla alternativa para casos sin diagnostico confirmado que no toleran la reintroducción de gluten.
Diagnóstico en adultos a dieta sin gluten
Existen dos perfiles de pacientes que requieren confirmación diagnóstica con la dieta sin gluten ya iniciada y que presentó Natalia López (Hospital Clínico San Carlos, Madrid). Unos la han iniciado por su cuenta sin pruebas previas y otros tienen pruebas previas con resultados no concluyentes. Para estos casos hay dos alternativas. Una es la prueba de provocación con gluten, que puede ser la estándar de 8 semanas si el paciente lo tolera bien o la corta de 3 días si no es así. En el primer caso se procedería con el protocolo habitual de diagnóstico transcurridas las 8 semanas. En el segundo caso se podría valorar la IL2 en sangre a las 4 horas de la primera ingesta, los linfocitos T CD4 en sangre al sexto día tras la primera ingesta (por tetrámeros o determinación de IFNgamma por ELISPOT, válidas sólo para sujetos DQ2.5) o los linfocitos T CD8 en sangre también al sexto día de la primera ingesta (por citometría de flujo, independiente del HLA del sujeto). La otra alternativa es una nueva biopsia para estudio de linfocitos intraepiteliales por citometría de flujo (linfograma intraepitelial), comprobando previamente que el estudio genético HLA es positivo (si es negativo, la EC queda descartada). En la práctica, lo más operativo es pautar la provocación corta para estudio de CD8 y extenderla a 8 semanas si el paciente lo tolera para biopsia con linfograma. Si no hay provocación, el linfograma es completo en el 45% de los casos, parcial en otro 45% y normal en el 10%.
Estudios comparativos
Cuando se comparan las biopsias de pacientes con las de sujetos sanos, éstas suelen corresponder en realidad a sujetos que se han sometido a una endoscopia por problemas digestivos diversos, como el reflujo gastroesofágico. Para comprobar si estos casos pueden utilizarse verdaderamente como controles sanos en los estudios comparativos, Albert Martí (Hospital Mutua de Terrassa, Barcelona) evaluó las biopsias de sujetos con reflujo y biopsias de sujetos completamente sanos. No se observaron diferencias en el recuento de mastocitos, eosinófilos ni de linfocitos intraepiteliales (un poco más altos en los casos con reflujo, pero dentro de los límites normales). La proporción de linfocitos T gamma-delta y CD3neg fue similar también.

Seguimiento de la enfermedad celíaca
Un estudio de intervención nutricional, presentado por Arrate Lasa (Universidad del País Vasco, Vitoria), ha seguido a 46 niños durante 1 año tras el diagnóstico de la EC. Durante este periodo se han recopilado datos antropométricos y bioquímicos en 3 visitas: al comienzo, a los 3 meses y al cabo de 1 año. Se ha recogido también información sobre síntomas digestivos y extradigestivos, así como de calidad de vida. Y se ha medido la adherencia la dieta sin gluten mediante el análisis de gluten en heces u orina en las diferentes visitas, todo ello acompañado de una orientación personalizada sobre alimentación y hábitos de vida. Los resultados de la intervención muestran una mejora en la adherencia a la dieta sin gluten y en los hábitos de alimentación, con una reducción de alimentos ultraprocesados, especialmente galletas, cuyo aporte calórico ha pasado del 24% al 17% de la ingesta total de calorías. También han mejorado los síntomas, tanto digestivos como extradigestivos, sobre todo anemia, cansancio y dolor de cabeza. La calidad de vida, en cambio, no se ha modificado, siendo mala en todo este periodo.
A pesar de tener un buen control dietético y nutricional, la persistencia de síntomas ocurre con cierta frecuencia en personas diagnosticadas de EC que ya llevan haciendo dieta sin gluten el tiempo suficiente para que se hubieran resuelto. Como mostró Jonatan Miranda (Universidad del País Vasco, Vitoria), no siempre son debidos al gluten por errores en la dieta sin gluten. En muchos casos son atribuibles a otros componentes alimenticios, como los carbohidratos fermentables (FODMAP, en el orden de gramos), los inhibidores de amilasa-tripsina (ATI, en el orden de miligramos), a la histamina (en el orden de miligramos) y a otros componentes, ya sea por ingesta insuficiente de elementos traza (cobre o zinc, en el orden de microgramos) o por ingesta elevada de contaminantes (níquel, en el orden de microgramos). No es raro que estas personas con síntomas digestivos diversos mejoren tras una reducción espontánea del aporte de FODMAP (en un 19%, equivalente a unos 4 gramos menos al día).
Por otro lado, la ausencia de síntomas no siempre es garantía de un buen control dietético y nutricional. En palabras de Ángeles Pizarro (Hospital Virgen del Rocío, Sevilla), el 70% de los pacientes con atrofia persistente son asintomáticos. Muchos de ellos no muestran elevación de anticuerpos en sangre. La ingesta de gluten es revelada por el análisis de gluten en heces y orina. En heces es detectable entre los 2 y los 7 días posteriores a la ingesta y en orina entre 1 y 6 horas después de la ingesta, llegando como mucho a las 36 horas.
En orina, la ingesta de 50 mg de gluten es detectada en el 56% de los casos (tomando las muestras a las 0, 7 y 17 horas), y 500 mg son detectados en el 86% de los casos. En heces, la cantidad ingerida se correlaciona con la cantidad detectada, según ensayos de provocación con diferentes cantidades de gluten (50 mg, 250 mg, 500 mg, 1 g). Estos estudios de provocación demuestran, además, que el 77% de los participantes cometían transgresiones antes del inicio de la prueba, cuando supuestamente su dieta sin gluten era estricta.
El protocolo de seguimiento sugerido para el control de la dieta sin gluten basado en estos métodos consistiría en analizar gluten en heces u orina en el momento del diagnóstico, a los 3 meses y a los 12 meses. La muestra inicial sería única en ambos casos (heces u orina) y para las siguientes determinaciones aconsejan 2 muestras de heces o 3 muestras de orina en la misma semana, recogidas en días alternos y pillando el fin de semana (por ejemplo, lunes-miércoles-sábado para la orina, jueves-domingo para las heces).
En pediatría, el análisis de gluten en heces es más adecuado para detectar transgresiones, según Carmen Ribes (Instituto de Investigación Sanitaria La Fe, Valencia). La excreción en orina cubre un marco temporal previo más corto y la dinámica de excreción puede ser variable por diferentes motivos.
Tratamiento: la dieta sin gluten
La Sociedad Europea de Gastroenterología, Hepatología y Nutrición Pediátrica (ESPGHAN) ha publicado recientemente un documento actualizando algunos aspectos relacionados con la dieta sin gluten que son objeto de controversia y que expuso Paula Crespo (Hospital Recoletas Campo Grande, Valladolid). La mayoría de estudios concluyen que el 30% de los pacientes cometen errores en la dieta sin gluten, que tienden a ser menos a medida que mejora el etiquetado de los productos. Por otro lado, la dieta sin gluten implica un déficit de fibra, folato, magnesio, selenio y vitamina D. Sobre posibles déficits de hierro y calcio hay resultados contradictorios. No obstante, estos desequilibrios nutricionales también van a menos. Sobre la avena, se considera seguro el consumo diario de 20-25 gr (peso seco, equivalente a una cucharada colmada) una vez transcurran 6 meses desde el diagnóstico. Y en cuanto al contacto cruzado, el hecho de compartir tostadora para panes con y sin gluten no parece repercutir en la seguridad de los pacientes.
Por otro lado, el grupo de investigación Gluten3S tiene habilitada una plataforma educativa sobre dieta sin gluten que permite además elaborar dietas sin gluten nutricionalmente equilibradas, con una opción de uso para particulares y otra para profesionales. Tal como explicó Gesala Pérez (Universidad del País Vasco, Vitoria), incorpora información nutricional de productos específicos sin gluten, datos obtenidos de más de 50 marcas comerciales. Incluye, además, productos que no son específicos sin gluten pero que son más habituales en las dietas sin gluten por el aporte de nutrientes que ofrecen en sustitución de los cereales con gluten y sus derivados, como el tofu o la quinoa. Incluye también información sobre el contenido en FODMAP y permite registrar datos de seguimiento antropométrico y bioquímico, así como realizar cuestionarios dietéticos y de calidad de vida.

Alimentos sin gluten
Pan sin gluten
Dos encuestas independientes sobre hábitos de consumo que se elaboran periódicamente, una del Instituto Nacional de Estadística (INE) y otra del Ministerio de Sanidad, concluyen, como indicó Paloma Castro (Instituto de Ciencia y Tecnología de Alimentos y Nutrición -ICTAN- del CSIC, Madrid), que se ha producido una caída notable en el consumo de pan en lo que va de siglo, pasando de 4,5 kg por persona al año en 2000 a 2,5 kg en 2023, y es menor en las personas más jóvenes. El consumo de pan sin gluten se evalúa desde 2020 y predomina en hogares unipersonales habitados por personas de mediana edad.
Olaia Martínez (Universidad del País Vasco, Vitoria) presentó los resultados de otra encuesta específica sobre los panes sin gluten que respondieron 265 personas con EC mayores de 18 años. Según se extrae de sus respuestas, opinan que son panes duros, desmigajados, de sabor raro y fuerte, además de caros. Los aspectos más críticos son la sequedad y la durabilidad. Para mejorar esto se estudió la mejora sensorial de panes básicos sin gluten elaborados a base de harinas de arroz, maíz y trigo sarraceno mediante la adición del mucílago extraído de semillas de lino y el bagazo de manzana, secado y triturado, que se genera como residuo en las sidrerías. Los panes obtenidos mejoran nutricionalmente (con más polifenoles, antioxidantes y fibra) pese al tratamiento térmico del pan, pero pueden perder cohesividad si se abusa a la hora de añadir ingredientes sensoriales. El impacto ambiental de estas fórmulas está balanceado dada la proximidad de las materias primas y por los residuos generados.
Por otro lado, panes elaborados con trigos obtenidos por ingeniería genética se investigan como alternativa. Helena Guzmán (Instituto de Agricultura Sostenible -IAS- del CSIC, Córdoba) presentó los resultados de un ensayo clínico realizado con pan elaborado con harinas derivadas de la línea de trigo transgénico E82, obtenida mediante ARNi. Su consumo por personas celíacas no dio lugar a activación inmunitaria a corto plazo en comparación con el pan de trigo estándar. Por su parte, ensayos de laboratorio con las líneas E82 y H329 mostraron una reducción en la liberación de IgE en sueros de pacientes con un tipo de alergia grave al trigo conocida como anafilaxia dependiente de trigo inducida por ejercicio. La tecnología CRISPR/Cas9, por su parte, se está empleando para mejorar el contenido proteico del arroz y las propiedades panificables de sus harinas incorporando prolaminas de trigo de 13 kilodalton y gluteninas A.
Cerveza sin gluten
Marian Bustamante (Universidad del País Vasco, Vitoria) recordó que la cerveza es la bebida fría más consumida fuera de casa (81% de la población de 18 a 65 años), y se ha estimado un crecimiento de mercado del 13,7% entre 2022 y 2028. La materia prima preferente es la cebada y el trigo, y como materias primas alternativas sin gluten se encuentran los cereales sin gluten, los pseudocereales y otras como la calabaza.
Si las materias primas tienen gluten, se puede reducir la toxicidad de la cerveza durante su elaboración, mediante procesos naturales como la fermentación, procesos físicos como la decantación, la filtración o la centrifugación, y procesos químicos como el tratamiento enzimático con transglutaminasas, prolil endopeptidasas o endoproteasas. Su comercialización como “cerveza sin gluten“ requiere el análisis de todos los lotes para garantizar su seguridad.
Este análisis, no obstante, tiene limitaciones. La cerveza es una matriz compleja en la que el gluten se encuentra hidrolizado (lo que dificulta su detección) y contiene polifenoles que interfieren en el proceso de extracción de gluten con etanol al 60%, que es necesaria para su análisis. El enzimoinmunoensayo ELISA basado en el anticuerpo R5 es el único aceptado legalmente para este análisis, aunque existen otros anticuerpos, como A1 y G12, que reconocen el péptido 33mer, o el anticuerpo alfa-20-gliadina, que se comprueba que ofrecen resultados dispares cuando son empleados en estudios comparativos. La cromatografía de flujo lateral, también basada en los anticuerpos R5, A1 o G12, permite igualmente detectar gluten y es más rápida.
No es sencillo averiguar si los síntomas que puede causar el consumo de cerveza son debidos a gluten residual no detectado o a otros componentes, como los carbohidratos fermentables (FODMAP), los inhibidores de amilasa-tripsina (ATI) o las aminas biógenas (histamina).
El análisis de gluten mediante inmunocromatografía en ensayos de flujo lateral con los anticuerpos A1 y G12, específicamente dirigidos contra el péptido 33mer, en comparación con el inmunoensayo convencional ELISA basado en el anticuerpo R5, muestra la discrepancia de resultados cuando se analizan cervezas etiquetadas “sin gluten” o “muy bajo en gluten”, ya estén elaboradas a partir de cereales con gluten, cereales con y sin gluten o cereales sin gluten, a raíz del estudio de 107 cervezas de diferentes países que expuso Verónica Segura (Universidad de Sevilla). María van der Hofstadt (Asociación de Celíacos de Europa -AOECS-) indicó que en España se comercializan actualmente 41 cervezas sin gluten certificadas.
Como candidatos alternativos a provocar los síntomas o inflamación intestinal ligados al consumo de cerveza sin gluten están los inhibidores de amilasa-tripsina (ATI). Silvia Matías (Universidad del País Vasco, Vitoria) explicó que son proteínas de defensa frente a plagas que se encuentran en cereales como trigo, cebada, centeno, maíz, arroz o mijo, en diferentes proporciones, y se vinculan con la activación de procesos inflamatorios intestinales. El análisis de ATI en 10 cervezas con gluten y 10 cervezas sin gluten muestra que en 7 de éstas últimas siguen estando presentes en cantidad relevante. El contenido en ATI se estima en base a su acción inhibitoria y se ha fijado de forma arbitraria una reducción del 40% de su actividad como límite para discriminar entre cervezas con y sin ATI.
Autor: Juan Ignacio Serrano Vela. Doctor en Biología. Servicio de Investigación y Formación de la Asociación.